皮肤作为人体最大的器官,承担着维持内环境稳态、抵御外界病原体入侵及感知外界刺激等重要生理功能。然而,因烧伤、创伤或慢性溃疡等导致的大面积皮肤缺损,往往伴随严重的功能障碍和并发症,其修复一直是临床医学和再生医学领域的重大挑战。目前,临床治疗主要依赖于自体皮肤移植、异体皮肤移植以及人工皮肤替代物等方法。然而,这些传统方法存在明显局限性。尽管组织工程技术的发展为皮肤再生提供了新思路,但现有方法在实现皮肤全层结构(包括表皮、真皮及附属器官)的功能性重建方面仍面临重大挑战。特别是如何构建具有生物活性的三维支架以模拟细胞外基质的复杂微环境,如何维持种子细胞的干性并引导其有序分化,以及如何促进新生组织的快速血管化和神经化等关键科学问题尚未得到有效解决。这些瓶颈严重制约着皮肤组织工程技术的临床转化和应用。因此,开发新型生物材料、优化细胞培养体系、构建仿生微环境已成为当前皮肤再生研究的重要方向,具有重要的科学意义和临床价值。
近日,我院动物多肽药物创制国家地方联合工程实验室陈海燕副教授课题组在期刊《Theranostics》(中科院一区Top,IF=12.4)上发表题为“3D bioprinting of prefabricated artificial skin with multicomponent hydrogel for skin and hair follicle regeneration”的研究文章。本研究聚焦于开发多模态响应型水凝胶支架,结合空间可控的3D生物打印技术,旨在构建具有细胞外基质拓扑特征及动态生化信号释放的仿生微环境,为实现皮肤全层结构及其毛囊、汗腺等附属器官的功能性再生提供创新解决方案。

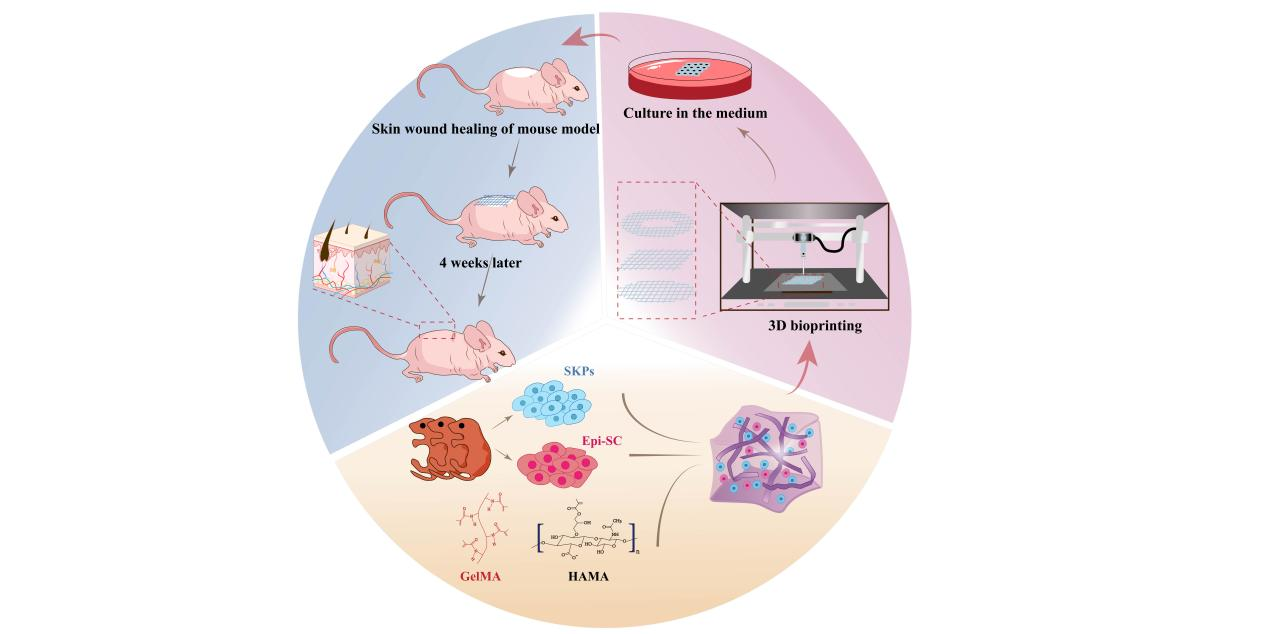
本研究创新性地采用3D生物打印技术,将皮肤源性前体细胞(SKPs)和表皮干细胞(Epi-SCs)精准植入GelMA/HAMA多模态响应型水凝胶中,成功构建出高精度人造皮肤。通过系统优化,确定5% GelMA-0.5% HAMA的最佳配比,该水凝胶体系展现出优异的溶解性、可控的溶胀率、良好的可打印性和理想的机械性能。深入的细胞学研究表明,该人造皮肤不仅能有效维持SKPs和Epi-SCs的细胞特性,还可显著上调SKPs中干性基因和毛囊诱导再生基因的表达水平。动物实验证实,移植4周后创面完全愈合,再生皮肤不仅重建了完整的表皮-真皮结构,还成功再生了毛囊、皮脂腺和血管结构,其组织结构与正常皮肤高度相似。更为让人兴奋的是,该人工皮肤在体外培养12小时后仍保持完整的功能性再生能力。这一突破性进展为伤口愈合、毛囊再生和含细胞人工皮肤的预制提供了创新性解决方案,同时为大规模伤口修复和附属器官再生领域开辟了新途径。此外,本研究建立的含细胞人工皮肤体外培养体系,为后续研究奠定了重要基础,具有很好的应用价值。
陈海燕副教授毕业于清华大学,一直从事再生医学的研究,利用生物3D打印与干细胞进行皮肤损伤等疾病的修复,相关研究成果发表在Nature communications、Acta Pharmaceutica Sinica B、Theranostics等期刊,先后获得国家自然科学基金、湖南省优青、江西省双千等科研项目7项;获得广东省自然科学奖二等奖、湖南省颠覆性技术大赛优秀项目奖等科研成果奖励;获得国家发明专利4项、申请国家发明专利9项。
该研究论文以我校为第一署名单位,硕士研究生马潇潇、朱肖慧为本文的共同第一作者,刘中华教授和陈海燕副教授为本文的通讯作者。本论文得到了湖南省自然科学基金、长沙市优秀青年科学基金等项目的支持。
原文链接:https://www.thno.org/v15p2933.htm


